( Khởi nghiệp với Internet)
Xem thêm: công cụ hỗ trợ tính Vt dựa trên cân nặng dự đoán (PBW) cho bệnh nhân thở máy hoặc Cài đặt máy thở ban đầu ở người lớn và Thở máy cho bệnh nhân hội chứng nguy kịch hô hấp cấp tính (ARDS)
Huy động phế nang không khuyến cáo sử dụng thường quy, mà chỉ được xem xét trong trường hợp ARDS trung bình đến nặng có P/F < 150 mmHg nhằm cải thiện quá trình oxy hóa. Đôi khi cũng có thể xem xét áp dụng ở bệnh nhân có biểu hiện giảm độ bão hòa oxy máu sau khi ngắt kết nối với máy thở (vận chuyển, thay hệ thống ống dây máy thở), khi hút đàm, nội soi phế quản, thay đổi lại tư thế bệnh nhân..điều mà có thể dẫn đến xẹp phế nang.
Blog tổng hợp những kinh nghiệm được học, áp dụng và chia sẻ
GIỚI THIỆU
Hội chứng suy hô hấp cấp tính (ARDS) là một dạng tổn thương phổi cấp tính, lan tỏa, viêm nhiễm có liên quan đến nhiều căn nguyên
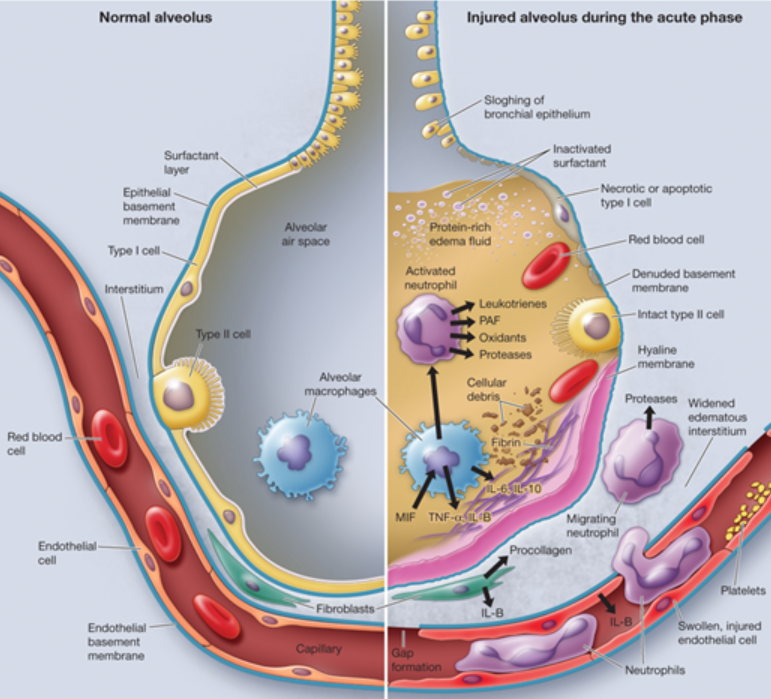
Sinh lý bệnh của ARDS chưa hoàn toàn được hiểu rõ. Khởi đầu, tổn thương phổi trực tiếp hoặc gián tiếp ngoài phổi làm gia tăng các chất trung gian viêm thúc đẩy tích tụ bạch cầu trung tính trong vi tuần hoàn phổi. Các bạch cầu trung tính này hoạt hoá và di chuyển với số lượng lớn trên bề mặt biểu mô nội mạc mạch máu và phế nang, giải phóng protease, các cytokine và các gốc oxy tự do (reactive oxygen species). Sự di chuyển và giải phóng các hóa chất trung gian dẫn đến tăng tính thấm mạch máu, khe hở trong hàng rào biểu mô phế nang, và hoại tử tế bào phế nang loại I và II. Điều này, đến lượt nó, dẫn đến phù phổi, hình thành màng hyaline và mất surfactant làm giảm độ đàn hồi của phổi và làm trao đổi khí khó khăn.Xâm nhập sau đó của nguyên bào sợi có thể dẫn đến lắng đọng collagen, xơ hóa, và làm bệnh trầm trọng hơn. Trong giai đoạn hồi phục, nhiều quá trình xảy ra đồng thời. Cytokine kháng viêm ngừng kích hoạt bạch cầu trung tính, sau đó trải qua quá trình chết theo chương trình và thực bào. Tế bào phế nang loại II tăng sinh và biệt hóa thành tế bào loại I, tái thiết lập sự toàn vẹn của niêm mạc biểu mô và tạo ra khuynh độ thẩm thấu kéo dịch ra khỏi phế nang và vào vi mạch phổi và bạch huyết phổi. Đồng thời, các tế bào phế nang và các đại thực bào dọn dẹp các protein từ phế nang giúp phổi phục hồi.
Nguyên nhân thường gặp
- Viêm phổi
- Hít dịch dạ dày
Nguyên nhân ít gặp
- Dập phổi
- Đuối nước
- Tổn thương phổi do hít khí độc
- Thuyên tắc do mỡ, do nước ối
- Phù phổi sau tái tưới máu do ghép phổi hay lấy huyết khối mạch phổi
Nguyên nhân thường gặp
- Nhiễm trùng huyết (sepsis)
- Chấn thương nặng với choáng và truyền máu nhiều lần
Nguyên nhân ít gặp
- Gãy nhiều xương
- Chấn thương đầu
- Bỏng nặng
- Truyền dịch quá mức
- Quá liều thuốc
- Viêm tụy cấp
- Thông nối tim phổi
- Truyền các chế phẩm máu
- Đông máu nội mạch lan tỏa
- Sốc phản vệ
- Bạch cầu cấp
Hội nghị Âu - Mỹ thống nhất về ARDS tại Berlin 2012
- Khởi phát đột ngột hoặc có các triệu chứng mới hoặc xấu đi trong vòng 7 ngày.
- X quang/ CT phổi có hình ảnh thâm nhiễm 2 bên (không do tràn dịch màng phổi, xẹp thùy phổi, xẹp phổi hoặc nốt phổi)
- Không có bằng chứng lâm sàng về tăng áp lực nhĩ trái (không do suy tim hoặc quá tải dịch)
- Giảm Oxy hóa máu khi thở máy PEEP ≥ 5 cmH2O:
- PaO2/FiO2: ≤ 300 nhẹ
- PaO2/FiO2: ≤ 200 trung bình
- PaO2/FiO2: ≤ 100 nặng
Ngoài 2 tiêu chí:
- Khởi phát đột ngột hoặc có các triệu chứng mới hoặc xấu đi trong vòng 7 ngày.
- Không có bằng chứng lâm sàng về tăng áp lực nhĩ trái (không do suy tim hoặc quá tải dịch).
- Siêu âm phổi(nếu người thực hiện được đào tạo tốt) được thêm vào để thay thế cho việc xác định thâm nhiễm 2 bên phổi dựa vào Xquang/ CT phổi.
- Để đánh giá oxy hóa máu: sử dụng oxy mũi lưu lượng cao (HFNO) ≥ 30 lít/phút (có ý nghĩa tương đương PEEP ≥ 5 cmH2O) và sử dụng chỉ số SpO2 (độ bảo hòa oxy đo bằng oxy xung mạch) thay cho PaO2 (trong khí máu động mạch) để xác định tình trạng giảm oxy hóa máu (được định nghĩa khi SpO2/FiO2 ≤ 315 mmHg với SpO2 ≤ 97% tương đương với PaO2/FiO2 ≤ 300 mmHg).
Và trong những bối cảnh có nguồn lực hạn chế để chẩn đoán ARDS thì không yêu cầu các tiêu chí liên quan đến: PEEP, HFNO (oxy lưu lượng cao), hoặc thiết bị hỗ trợ hô hấp chuyên biệt (thở máy không xâm lấn (NIV/CPAP) hoặc thở máy xâm lấn). Xem thêm: Định nghĩa toàn cầu mới về ARDS 2023
- Phù phổi do tim
- Chảy máu phế nang lan tỏa
- Viêm phổi kẽ cấp tính
- HC Mamman-Rich
- Viêm phổi do tăng BC ái toan
- Lao phổi
- Viêm phổi tổ chức hóa không rõ nguyên nhân
- Ung thư di căn lan tỏa
Trong bối cảnh lâm sàng việc loại trừ phù phổi cấp do tim thường dựa vào đánh giá lâm sàng, xét nghiệm BNP hoặc NT-proBNP, siêu âm tim qua thành ngực (TTE).
- Đánh giá lâm sàng: Phù do tim thường do rối loạn chức năng tâm thu hoặc tâm trương thất trái, nhưng cũng có thể do quá tải dịch, tăng huyết áp nặng hoặc bệnh thận nặng. Bằng chứng về rối loạn chức năng tim (tiếng ngựa phi T3 hoặc T4, tiếng thổi mới hoặc thay đổi), áp lực đổ đầy tim phải tăng cao (tĩnh mạch cổ nổi, phù chân) hoặc có các bất thường trên X quang (xung huyết tĩnh mạch phổi, đường Kerley B, bóng tim to, hoặc dịch màng phổi). Đáp ứng với điều trị lợi tiểu cũng có thể xác nhận chẩn đoán hồi cứu.
- BNP hoặc NT-proBNP: chỉ riêng BNP nói chung không đáng tin cậy để phân biệt, mà cần phải kết hợp với đánh giá lâm sàng. BNP máu < 100 pg/mL xác định ARDS có độ nhạy 27% và độ đặc hiệu 95%. Do đó, BNP < 100 pg/mL có thể có lợi cho việc chẩn đoán ARDS, nhưng mức cao hơn không xác nhận suy tim cũng như không loại trừ ARDS.
- Siêu âm tim qua thành ngực (TTE): ở những bệnh nhân nghi ngờ ARDS(không áp dụng thường quy nếu ít nghi ngờ), TTE có thể thực hiện để tìm kiếm bằng chứng về rối loạn chức năng tim khi không thể loại trừ phù phổi do tim bằng đánh giá lâm sàng, kết quả xét nghiệm và hình ảnh Xquang/CT. Phân suất tống máu (EF) bình thường thường có lợi cho chẩn đoán ARDS, trong khi rối loạn chức năng van động mạch chủ hoặc van hai lá nghiêm trọng, rối loạn chức năng tâm trương nghiêm trọng hoặc phân suất tống máu thất trái(LVEF) giảm nặng có thể dẫn đến phù phổi cấp do tim. Tuy nhiên, sốc nhiễm trùng có thể gây viêm cơ tim cấp tính đồng thời với ARDS, hoặc phù phổi do quá tải thể tích(truyền máu, hồi sức dịch) gây tổn thương phổi cấp ở bệnh nhân có chức năng tim bình thường, tổn thương phổi cấp do quá tải thể tích biểu hiện bằng áp lực động mạch phổi bít tăng cao(PCWP > 18 mmHg) khi đặt catheter động mạch phổi.
- Siêu âm Doppler qua thực quản: cho thấy giảm chỉ số tim (CI) và tăng thời gian lưu lượng hiệu chỉnh (FTc) phù hợp với phù phổi do tim.
Giai đoạn xuất tiết sớm trong 7 đến 10 ngày đầu tiên là một phản ứng không đặc hiệu đối với tổn thương phổi do nhiều nguyên nhân được đặc trưng bởi phù nề kẽ, viêm cấp tính và mãn tính, tăng sản tế bào loại II và hình thành màng hyalin.
Sau khoảng 7 đến 10 ngày, giai đoạn tăng sinh phát triển, đặc trưng bởi sự phân giải phù phổi, tăng sinh tế bào phế nang loại II, chuyển sản vảy, thâm nhiễm kẽ bởi nguyên bào sợi và sự lắng đọng sớm của collagen. Không biết giai đoạn này kéo dài bao lâu nhưng có lẽ trong khoảng từ hai đến ba tuần.
Một số bệnh nhân tiến triển đến giai đoạn xơ hóa, được đặc trưng bởi sự phá hủy cấu trúc phổi bình thường, xơ hóa và hình thành bao nang. Mức độ xơ hóa từ tối thiểu đến nặng.
Xem phần nguyên nhân ở trên
- Nhận diện và điều trị các bệnh lý nguyên nhân
- Thông khí cơ học với chế độ bảo vệ phổi
- Cân bằng nước dịch
- Giảm thiểu biến chứng của điều trị và các thủ thuật
- Dự phòng huyết khối tĩnh mạch, xuất huyết tiêu hóa, hít sặc, tránh thuốc an thần quá mức, tránh nhiễm trùng
- Cung cấp đầy đủ dinh dưỡng.
Với việc oxy mũi lưu lượng cao (HFNO) ngày càng được sử dụng phổ biến, có thể xem xét việc sử dụng HFNO để giảm nhu cầu đặt nội khí quản. Tuy nhiên, HFNO có nên thay thế cho thở máy không xâm lấn NIV/CPAP hay không hoặc có thể sử dụng chỉ số ROX để xác định thời điểm HFNO thất bại và cần đặt nội khí quản hay không hiện chưa có khuyến cáo rõ ràng.
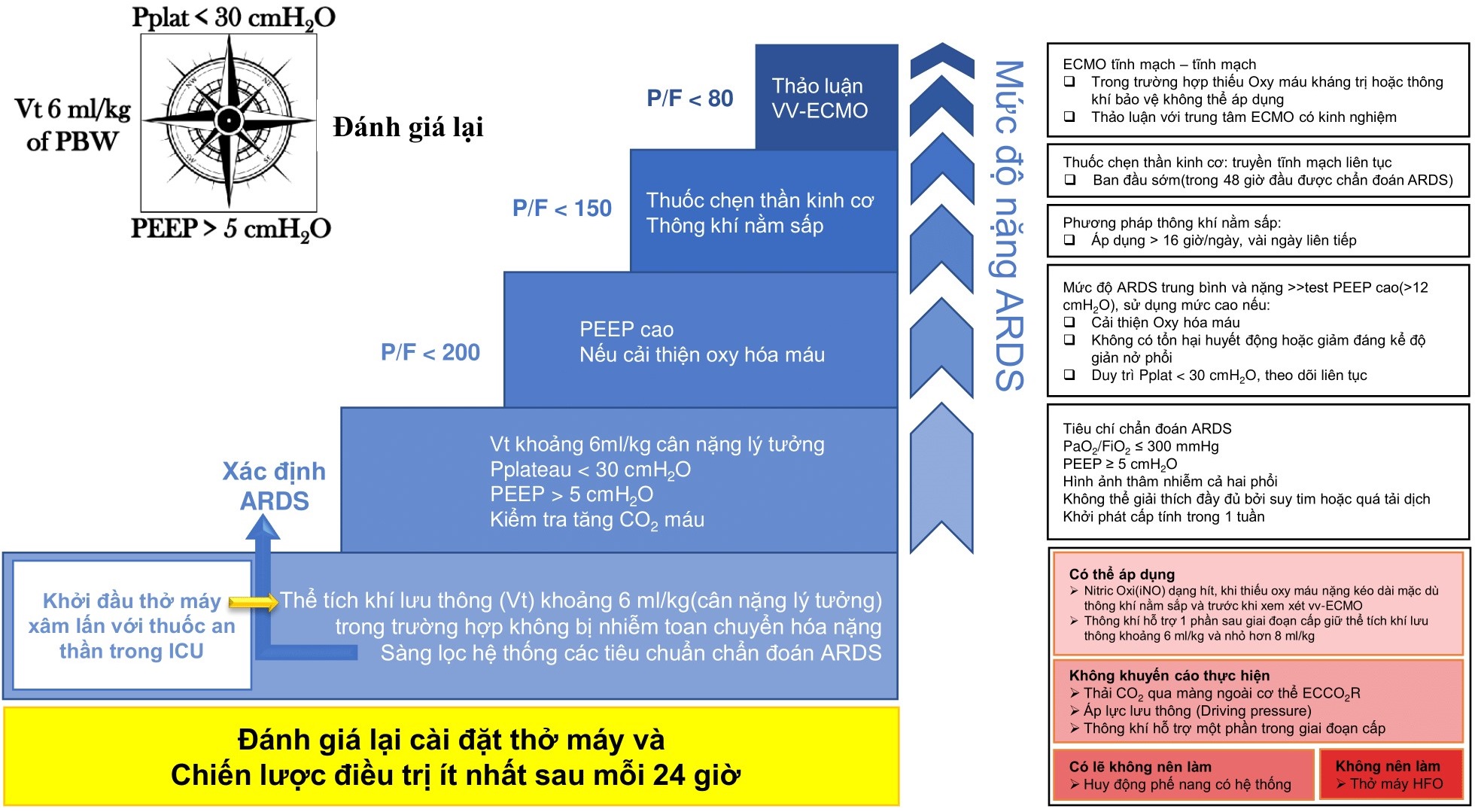
Thông khí bảo vệ phổi đề cập đến thể tích khí lưu thông(Vt) thấp từ 4 - 8 ml/kg (cân nặng dự đoán) và áp lực bình nguyên Pplat < 30 cmH2O vẫn là nền tảng trong quản lý ARDS để giảm thiểu tổn thương phổi gây ra bởi thở máy (Ventilator-induced Lung Injury - VILI). Một yếu tố quan trọng khác của thông khí bảo vệ phổi là sử dụng áp lực dương cuối thì thở ra (PEEP) để cải thiện tình trạng thiếu oxy và hạn chế xẹp phổi. Xem thêm: Thở máy cho bệnh nhân hội chứng nguy kịch hô hấp cấp tính (ARDS)
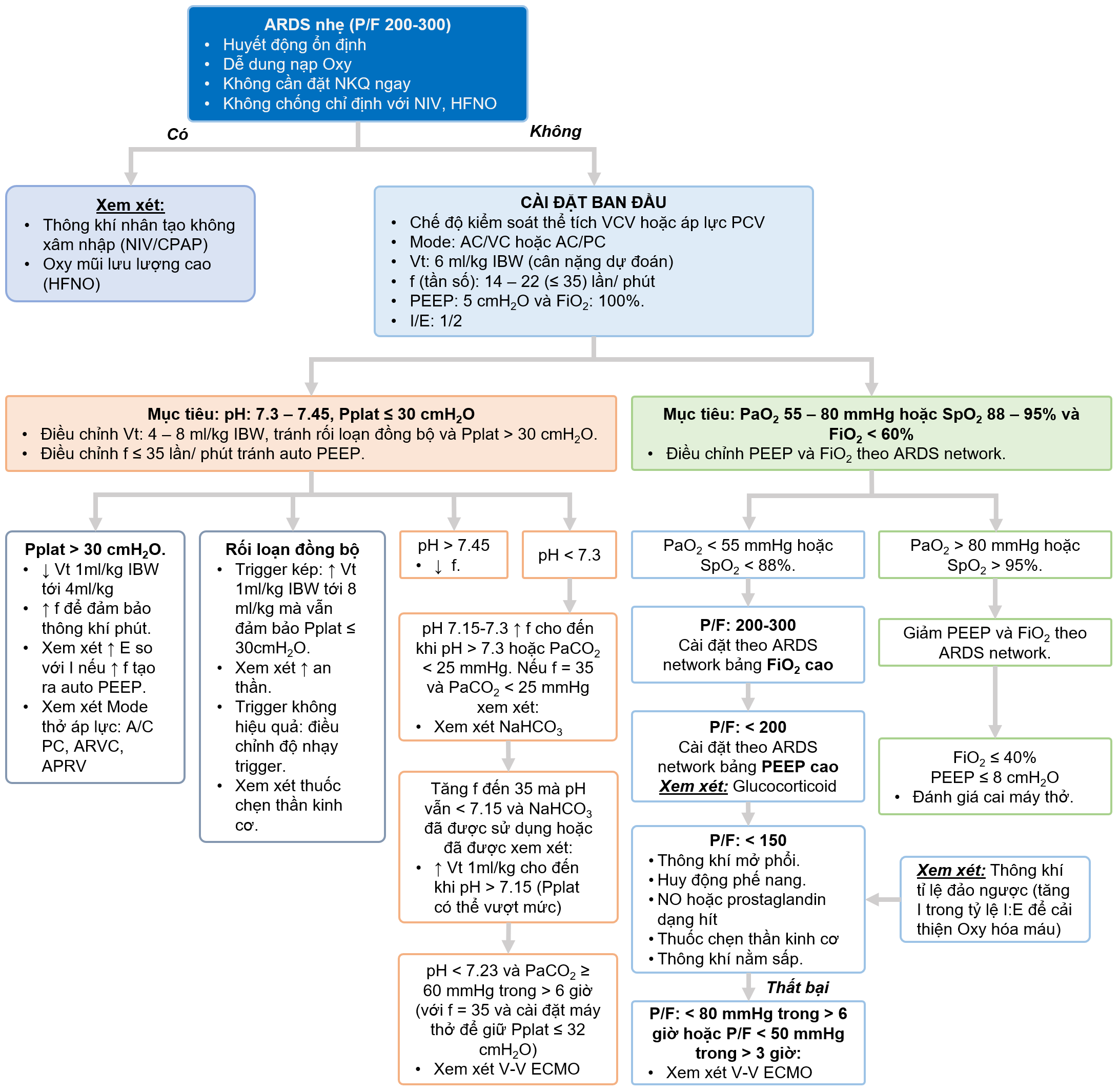
- PaO2 : 55 – 80 mmHg hoặc SpO2: 88 – 95% và duy trì FiO2 < 60%
- Bằng cách: tăng PEEP và FiO2 theo ARDS network
- Khi FiO2 > 70% hoặc Pplat > 30 cmH2O mà PaO2 < 55 mmHg hoặc SpO2 < 88%: sử dụng các biện pháp cứu cánh bổ sung: thông khí mở phổi, huy động phế nang,...
- Nếu Pplat > 30 cmH2O bằng cách: giảm Vt 1ml/kg có thể đến mức 4ml/kg
- Nếu Pplat < 25 cmH2O và Vt <6 mL/kg(cân nặng lý tưởng), tăng Vt thêm 1 mL/kg IBW cho đến khi Pplat > 25 cmH2O (mà Pplat vẫn ≤ 30 cmH2O) hoặc Vt = 6 mL / kg (hoặc 7 đến 8 ml/kg IBW nếu rối loạn đồng bộ máy thở [đói khí] nghiêm trọng, nếu Pplat vẫn còn ≤ 30 cmH2O).
- Nếu pH 7.15 - 7.30 tăng tần số thở(f) cho đến khi pH > 7.3 hoặc PaCO2 < 25 mmHg (xem xét NaHCO3 nếu f = 35 và PaCO2 < 25 mmHg)
- Nếu pH < 7.15 tăng f đến 35: nếu pH vẫn < 7.15 và NaHCO3 được sử dụng hoặc được xem xét, tăng Vt thêm 1 mL/kg cho đến khi pH > 7.15 (Pplate có thể vượt mức).
Để tìm Pplat trên máy thở R860 có 2 cách:
- Đo Pplat ngắt quãng: sử dụng chức năng Insp Hold: chọn time 2 giây và play.
- Đo Pplat liên tục: sử dụng Mode A/C VC, thiết lập Insp Pause sau cho Tpause = 10% thời gian của 1 chu kỳ thở. Với thời gian của 1 chu kỳ thở = 60/tần số thở.
- Mode: kiểm soát thể tích VCV như AC/VC, có thể sử dụng Mode áp lực PCV như AC/PC miễn đạt được Vt mong muốn.
- Vt ban đầu: 6 ml/kg cân nặng lý tưởng (IBW), điều chỉnh Vt dựa theo Pplat ở trên.
- PEEP: 5-10 cmH2O (điều chỉnh cùng với FiO2 theo ARDS Network)
- Tần số thở 14 - 22 lần/phút (≤35 lần/ phút)
- I:E khoảng 1:2 (khoảng điều chỉnh 1:1-1:3)
- FiO2: 100%
Cài FiO2 và PEEP Theo ARDS Network
| ARDS nhẹ (PaO2/FiO2: ≤ 300 mmHg) | ||||||||
|---|---|---|---|---|---|---|---|---|
| FiO2 | 0.3-0.4 | 0.4-0.5 | 0.5-0.6-0.7 | 0.7 | 0.7-0.8-0.9 | 0.9 | 0.9 | 1.0 |
| PEEP | 5 | 8 | 10 | 12 | 14 | 16 | 18 | 18-24 |
| ARDS trung bình đến nặng (PaO2/FiO2: ≤ 200 mmHg) | ||||||
|---|---|---|---|---|---|---|
| FiO2 | 0.3 | 0.4 | 0.5 | 0.5-0.8 | 0.8-0.9-1.0 | 1.0 |
| PEEP | 5-8-10-12-14 | 14-16 | 16-18 | 20 | 22 | 24 |
Khi PaO2/FiO2 < 150
- Thuốc chẹn thần kinh cơ(truyền liên tục) bắt đầu trong 48 giờ đầu (kéo dài không quá 48 giờ)
- Thông khí nằm sấp nên được thực hiện ít nhất 16 giờ liên tục/ ngày.
Khuyến cáo
- Nitrogen Monoxide (NO) có thể được sử dụng trong trường hợp giảm Oxy hóa máu nặng mặc dù đã thực hiện chiến lược thông khí bảo vệ phổi và thông khí nằm sấp và trước khi dự tính sử dụng ECMO v-v.
- Cân nhắc ECMO khi PaO2/FiO2 < 150 và/ hoặc thở máy trở nên nguy hiểm khi Pplate tăng cao mặc dù đã tối ưu hóa PEEP cao, thuốc chặn thần kinh cơ và thông khí nằm sấp. Quyết định ECMO cần được đánh giá sớm bằng cách liên hệ với với chuyên gia
- Sau giai đoạn cấp có thể sử dụng MODE hỗ trợ áp lực đảm bảo Vt 6 - 8 ml/kg
Không khuyến cáo
- Không khuyến cáo thông khí tự thở (nhịp thở SPONT) thường quy trong giai đoạn cấp ARDS.
- Thông khí dao động tần số cao (HFO: cung cấp Vt nhỏ 1-3 mL/kg với tần số 3-6Hz và áp lực trung bình đường thở cao, mục đích tạo thuận lợi để mở các phế nang và hạn chế xẹp phổi, cải thiện trao đổi oxy và thải CO2) không nên sử dụng vì các nghiên cứu cho thấy không có lợi và tác hại có thể xảy ra.
- Dữ liệu hiện có chưa khuyến cáo sử dụng thiết bị loại bỏ CO2 qua màng ngoài cơ thể.
Cai máy thở khi: PEEP ≤ 8, FiO2: ≤ 40%. Xem thêm: Cai an thần và cai thở máy
Theo hướng dẫn của Hiệp hội Lồng ngực Anh (ATS) khuyến nghị ECMO ở một số bệnh nhân ARDS nặng đang thông khí bảo vệ phổi với điểm MURRAY > 3 hoặc PH < 7,2 do tăng CO2 máu mất bù. Tuy nhiên, không có khuyến cáo nào chắc chắn ủng hộ hoặc phản đối ECMO trong ARDS nặng trong hướng dẫn của ATS/ Hiệp hội Hô Hấp Châu Âu (ERS)/ Hiệp hội Y học Hồi sức tích cực (SCCM).
ECMO ngày càng được sử dụng tăng lên như một giải pháp cứu cách cho liệu pháp cải thiện Oxy hóa máu, có thể thích hợp đối với bệnh nhân ARDS nặng thất bại với chiến lược thông khí Vt thấp tiêu chuẩn, thất bại hoặc không thích hợp để thông khí nằm sấp và chiến lược PEEP cao/ huy động phế nang. Cần xem xét một số chống chỉ định. Điều quan trọng là nên được áp dụng sớm (trong vòng 7 ngày) là rất quan trọng trong sự thành công của ECMO. Do đó, những trung tâm không có ECMO nên chuyển viện sớm đến trung tâm có ECMO.
Các tiêu chí cho ECMO:
- P/F < 50 mmHg trong > 3 giờ.
- P/F < 80 mmHg trong > 6 giờ.
- pH < 7,25 và PaCO2 ≥ 60 mmHg trong > 6 giờ (với tần số thở f ở mức 35 nhịp/phút và cái đặt máy thở để giữ Pplat ≤ 32 cmH2O)
Được khuyến cáo cho bệnh nhân ARDS trung bình nặng (P/F < 150 mmHg và PEEP ≥ 5 cmH2O) mặc dù đã tối ưu hóa thông khí để giảm tỷ lệ tử vong. Nằm sấp nên được áp dụng liên tục > 16 giờ/ngày(18-20 giờ/ngày) trong vài ngày và điều quan trọng là phải áp dụng sớm (trong vòng 7 ngày). Nếu bệnh nhân không cải thiện (ví dụ: sau 6 - 8 giờ và đôi khi đến 20 giờ thông khí nằm sấp) nên xem xét các biện pháp khác tiếp theo.
Các chống chỉ định:
- Vết thương hở/ vết bỏng trên bề mặt cở thể vùng bụng
- Các gãy xương không ổn định
- Mất ổn định cột sống
- Tăng áp lực nội sọ (ICP)
- Huyết động không ổn định
Thận trọng nếu: mở khí quản, đặt ống dẫn lưu màng phổi, béo phì, cổ chướng.
Thủ thuật huy động phế nang là việc áp dụng áp lực đường thở dương liên tục (CPAP) hay PEEP ở mức độ cao với mục tiêu huy động những phần của phổi không được trao đổi khí liên quan đến ARDS để tham gia vào trao đổi khí.
Thủ thuật huy động phế nang 40/40: Đặt mức áp lực CPAP hoặc PEEP: từ 35 - 40 cmH2O với thời gian trong 40 giây. Mức PEEP sau đó được chuẩn độ trên mức PEEP thường dùng ≥ 2 cmH2O nhưng thấp hơn mức PEEP dùng trong thủ thuật huy động phế nang, hoặc đặt PEEP theo FiO2 trong bảng ARDS network có mức PEEP cao. Hầu hết các chuyên gia đều thực hiện trong giai đoạn sớm của ARDS (tức giai đoạn xuất tiết sớm: 7 - 10 ngày đầu). Và thực hiện một lần, có thể lặp lại hơn một lần nếu đáp ứng được quan sát thấy nhưng chỉ duy trì thoáng qua. (xem thêm: Huy động phế nang CPAP 40/40)
Tác dụng phụ phổ biến của thủ thuật huy động phế nang là hạ huyết áp và giảm độ bão hoà oxy. Nhưng những ảnh hưởng này thường tự giới hạn và không có hậu quả nghiêm trọng. Tuy nhiên, có thể có một số nguy cơ chấn thương phổi do áp lực và ngừng tim khi thực hiện thủ thuật huy động phế nang trong thời gian dài. Cần phải theo dõi cẩn thận tình trạng mất ổn định huyết động bất cứ khi nào thực hiện thủ thuật này.
Sử dụng thông khí Vt thấp(6 mL/kg) kết hợp PEEP tăng dần (2-3 cmH2O) để đo độ giãn nở phổi động Cdyn sau mỗi 3 - 5 phút (thời gian để huy động phế nang), SpO2 và huyết áp. Để tìm ra mức Cdyn cao nhất mà Pplat ≤ 30 cmH2O, đồng thời cải thiện SpO2 tốt nhất, mức PEEP tương ứng với Cdyn đó được chọn là PEEP tối ưu dùng để thiết lập.
Cân bằng dịch dương tối thiểu hoặc cân bằng dịch âm với mục tiêu hợp lý là:
- CVP < 4 mmHg (qua catheter tĩnh mạch trung tâm CVC) hoặc
- PAOP < 8 mmHg (qua catheter động mạch phổi PAC)
- MAP > 60 mmHg khi không sử dụng thuốc vận mạch
- Lượng nước tiểu ≥ 0,5 mL/kg/giờ
- Bằng chứng về tuần hoàn đầy đủ dựa trên khám lâm sàng hoặc chỉ số tim (CI) ≥ 2,5 L/phút/m2da.
Thuốc lợi tiểu và hạn chế dịch là chiến lược để thực hiện mục tiêu này. Trong trường hợp cần sử dụng dịch(MAP < 60 mmHg) như sốc giảm thể tích hoặc sốc nhiễm trùng, ưu tiên sử dụng dịch tinh thể cân bằng.
Bệnh nhân cần được thiếp lập đường truyền tĩnh mạch trung tâm và đo huyết áp động mạch xâm lấn để theo dõi CVP, MAP và CI (chỉ số tim). Ở bệnh nhân MAP < 60 mmHg: cần tối ưu huyết động với truyền dịch, vận mạch đến khi MAP ≥ 60 mmg mà không cần sử dụng đến vận mạch (ngoại trừ Dopamine < 5 mcg/kg/phút) và tiếp tục tối ưu mục tiêu như sau:
Nếu Furosemide không có sẵn có thể thay thế bằng dumetanide với tỷ lệ quy đổi 40:1 (furosemide 40 mg = bumetanide 1 mg).
Bolus dịch lý tưởng nhất được cho ở những bệnh nhân được chứng minh đáp ứng với truyền dịch bằng cách sử dụng phương pháp thăm dò động khách quan để giảm thiểu việc sử dụng dịch tinh thể hoặc dịch keo một cách không cần thiết, Bệnh nhân được xem xét đáp ứng với truyền dịch nếu thay đổi áp lực mạch (PPV) giảm < 13%, chỉ số giãn IVC theo hô hấp giảm < 18%, và thay đổi chỉ số thể tích nhát bóp tăng lên > 10%. Xem thêm phần theo dõi huyết động.
| CVP | Lượng nước tiểu trung bình <0.5 mL/kg/giờ | Lượng nước tiểu trung bình ≥0.5 mL/kg/giờ | ||
|---|---|---|---|---|
| CI < 2.5 hoặc chi lạnh, nổi vân tím với thời gian đổ đầy mao mạch ≥ 2 giây | CI ≥ 2.5 hoặc không có bằng chứng của suy giảm tuần hoàn | CI < 2.5 hoặc chi lạnh, nổi vân tím với thời gian đổ đầy mao mạch ≥ 2 giây | CI ≥ 2.5 hoặc không có bằng chứng của suy giảm tuần hoàn | |
| CVP > 13 | 1/ Dopamine Furosemide |
5/ Furosemide | 9/ Dopamine Furosemide |
13/ Furosemide |
| CVP 9-13 | 2/ Dopamine | 6/ Furosemide | 10/ Dopamine | 14/ Furosemide |
| CVP 4-8 | 3/ Bolus dịch | 7/ Bolus dịch | 11/ Bolus dịch | 15/ Furosemide |
| CVP < 4 | 4/ Bolus dịch | 8/ Bolus dịch | 12/ Bolus dịch | 16/ Giữ thông tĩnh mạch(vein) |
| Với các ô: 1,5,6 Furosemide với liều 20 mg bolus IV, hoặc truyền IV với tốc độ 3 mg/giờ. NGỪNG DÙNG nếu Creatinine > 3 mg/dL hoặc Creatinine 0-3 mg/dL với xét nghiệm khác phù hợp với suy thận, hoặc sử dụng thuốc vận mạch/ bolus dịch trong 12 giờ qua. |
Đánh giá lại trong 1 giờ: Gấp đôi liều Furosemide hàng giờ cho đến khi lượng nước tiểu ≥ 0.5 mL/kg/giờ hoặc đạt liều tối đa 24 mg/giờ hoặc liều bolus 160 mg. Ngừng Furosemide nếu không đáp ứng. |
| Với các ô: 9,13,14,15 Furosemide với liều 20 mg bolus IV, hoặc truyền IV với tốc độ 3 mg/giờ. NGỪNG DÙNG nếu Creatinine > 3 mg/dL hoặc Creatinine 0-3 mg/dL với xét nghiệm khác phù hợp với suy thận, hoặc sử dụng thuốc vận mạch/ bolus dịch trong 12 giờ qua. |
Đánh giá lại trong 4 giờ: nếu vẫn trong ô có chỉ định cho Furosemide, cho một liều tương đương nếu lượng nước tiểu > 3 mL/kg/giờ, gấp đôi liều nếu lượng nước tiểu ≤ 3 mL/kg/giờ, đạt liều tối đa 24 mg/giờ hoặc liều bolus 160 mg. Ngừng Furosemide nếu không đáp ứng. |
| Với các ô: 3,4,7,8 cho nước muối sinh lý, dịch tinh thể cân bằng (Plasmalyte), hoặc Ringer lactate bolus 15 mL/kg, 1 đơn vị hồng cầu khối hoặc 25 g Albumin 25%. | Đánh giá lại trong 1 giờ. Cho tới 3 liều bolus trong 24 giờ nếu được chỉ đinh trong ô. |
| Với các ô: 11,12 cho nước muối sinh lý, dịch tinh thể cân bằng (plasmalyte) hoặc Ringer lactate bolus 15 mL/kg, 1 đơn vị hồng cầu khối hoặc 25 g Albumin 25%. | Đánh giá lại trong 4giờ. Thêm liều bolus theo chỉ định của bác sĩ điều trị. |
| Với các ô: 1,2,9,10 Dopamine bắt đầu với liều 5 mcg/kg/phút. | Tăng lên 5 mcg/kg/phút cho đến khi CI > 2.5 |
Nếu Furosemide không có sẵn có thể thay thế bằng dumetanide với tỷ lệ quy đổi 40:1 (furosemide 40 mg = bumetanide 1 mg).
Ngừng điều trị thuốc lợi tiểu trong suy thận (được định nghĩa là phụ thuộc vào lọc máu, thiểu niệu với Creatinine > 3 mg/dL, hoặc thiểu niệu với Creatinine 0-3 mg/dL với chỉ số tiết niệu cho thấy suy thận cấp) và ngừng cho đến 12 giờ sau khi dùng liều bolus dịch hoặc thuốc vận mạch cuối cùng.
Bolus dịch lý tưởng nhất được cho ở những bệnh nhân được chứng minh đáp ứng với truyền dịch bằng cách sử dụng phương pháp thăm dò động khách quan để giảm thiểu việc sử dụng dịch tinh thể hoặc dịch keo một cách không cần thiết, Bệnh nhân được xem xét đáp ứng với truyền dịch nếu thay đổi áp lực mạch (PPV) giảm < 13%, chỉ số giãn IVC theo hô hấp giảm < 18%, và thay đổi chỉ số thể tích nhát bóp tăng lên > 10%. Xem thêm phần theo dõi huyết động.
Hiệu quả của thuốc chẹn thần kinh cơ (sử dụng cisatracurium trong 48 giờ) trong các thử nghiệm (ACURASYS 2010, ROSE 2019) ở bệnh nhân ARDS có mức P/F < 150 mmHg cho thấy không giảm tỷ lệ tử vong đáng kể so với giả dược. Trong thử nghiệm ACURASYS 2010 dữ liệu sau khi được điều chỉnh có giảm tỷ lệ tử vong trong 90 ngày ở nhóm bệnh nhân ARDS nặng P/F < 120 mmHg, giảm được số ngày thở máy và ít khả năng bị chấn thương phổi do áp lực hơn đáng kể trong 28 và 90 ngày so với giả dược.
Vì vậy, không khuyến cáo sử dụng thường quy thuốc chẹn thần kinh cơ(NMB) cho bệnh nhân ARDS. Với dữ liệu hiện tại, có thể xem xét sử dụng cho bệnh nhân ARDS:
- Giảm oxy máu nặng kháng trị với các liệu pháp tiêu chuẩn
- Những bệnh nhân rối loạn đồng bộ máy thở nghiêm trọng đã kháng trị với điều chỉnh máy thở và an thần, đặc biệt là dẫn đến kích hoạt kép (ví dụ: di chuyển vận động không mong muốn, chẳng hạn như run rẩy do hạ thân nhiệt).
NMB giúp tạo điều kiện thuận lợi cho thông khí cơ học: tăng độ giãn nở thành ngực, ngăn ngừa các cử động hô hấp phối hợp kém, giảm áp lực đỉnh đường thở, và tạo điều kiện thuận lợi cho việc tăng CO2 ở mức cho phép.
Tuy nhiên, cần cân nhắc những bất lợi của việc phối hợp NMB với glucocorticoid, vì cả hai thuốc này đều liên quan đến sự phát triển bệnh cơ và bệnh đa dây thần kinh nghiêm trọng.
Xem thêm liều lượng thuốc: An thần, giảm đau, giãn cơ ở bệnh nhân thở máy trong ICU.
Thuốc giãn mạch phổi dạng hít có khả năng làm giãn mạch có chọn lọc các mạch máu ở vùng phổi được tưới máu tốt, dẫn đến cải thiện oxy hóa do tương xứng thông khí/tưới máu(V/Q) tốt hơn và cũng có thể góp phần cải thiện thiếu oxy ở bệnh nhân tăng áp phổi. Do đó, ở những bệnh nhân ARDS nặng bị giảm oxy máu kháng trị với các liệu pháp điều trị tiêu chuẩn, thuốc giãn mạch phổi dạng hít (Oxit nitric [NO] hoặc prostaglandin [prostacyclin như eporostenol, iloprost]) có thể được sử dụng để cải thiện quá trình oxy hóa. Đặc biệt hữu ích ở bệnh nhân ARDS có tăng áp động mạch phổi mất bù hoặc cấp tính và rối loạn chức năng tim phải. Tuy nhiên, chúng chưa cho thấy làm giảm tỷ lệ bệnh tật và tử vong, cũng như đáp ứng là không chắc chắn, và tác dụng phụ tiềm ẩn có thể xảy ra:
- NO: hạ huyết áp, methemoglobin máu, suy thận
- Prostacyclin: hạ huyết áp, đau ngực, chảy máu, đỏ bừng da, đau đầu, buồn nôn và nôn ói.
Đánh giá đáp ứng trong vòng 24 giờ đầu tiên
- Đáp ứng đáng kể chẳng hạn như cải thiện P/F từ 10 - 20 % trở lên, với trường hợp đáp ứng tiếp tục sử dụng nhưng tránh kéo dài (ví dụ vài ngày, nhất là NO).
- Không đáp ứng: ngừng sử dụng.
Lựa chọn thuốc, tùy tính sẵn có của cơ sở y tế, chi phí NO dạng hít cao hơn, nhưng thường có sẵn ở cơ sở chăm sóc nhi khoa sơ sinh có tăng áp phổi:
- NO dạng hít: một số phân tích tổng hợp cho thấy cải thiện oxy hóa máu khiêm tốn, thoáng qua mà không cải thiện tỷ lệ tử vong, thời gian thở máy hoặc số ngày không thở máy khi so sánh với giả dược hoặc điều trị thông thường. Tuy nhiên, các nghiên cứu hồi cứu gợi ý rằng những bệnh nhân không bị nhiễm trùng huyết mà có sức cản mạch phổi nền cao, và những bệnh nhân đáp ứng với PEEP có thể tăng khả năng đáp ứng với NO dạng hít. NO dạng hít được sử dụng bằng cách trọn NO và oxy có áp suất thấp và điều chỉnh lưu lượng NO bằng van, cung cấp cho bệnh nhân bằng mặt nạ chuyên dụng hoặc dạng ngạnh mũi ở bệnh nhân thở tự nhiên hoặc qua máy thở cho bệnh nhân thở máy. Khi sử dụng trong hơn vài ngày, không nên ngừng thuốc đột ngột mà phải giảm liều từ từ (giảm 10/triệu trong vài ngày), đến khi đạt liều 10/triệu có thể ngừng sử dụng.
- Prostaglandin dạng hít: cải thiện oxy hóa máu và giảm áp động mạch phổi trong 25 nghiên cứu. Ưu điểm của prostacyclin so với NO là không yêu cầu thiết bị phức tạp để sử dụng. Lưu ý, không ngừng thuốc đột ngột, khi muốn ngừng thuốc nên giảm liều từ từ (ví dụ: 10 ng/kg/giờ).
- Liều cố định, hít liên tục: bắt đầu: sử dụng dung dịch 20.000 ng/mL và phun khí dung với tốc độ 8 mL/giờ, điều chỉnh giảm dần liều dựa trên đáp ứng lâm sàng bằng cách giảm xuống 10.000 ng/mL trong khi tiếp tục phun khí dung với tốc độ 8 mL/giờ, ngừng thuốc dựa trên đáp ứng lâm sàng.
- Liều dựa trên cân nặng: cách 1: Hít liên tục, bắt đầu: 50 ng/kg/phút (sử dụng cân nặng lý tưởng); điều chỉnh giảm liều bằng cách giảm 10 mg/kg/phút sau mỗi 1 - 4 giờ dựa trên đáp ứng lâm sàng; liều tối đa 50 ng/kg/phút. HOẶC cách 2: hít liên tục, bắt đầu 10 ng/kg/phút (sử dụng cân nặng lý tưởng), điều chỉnh liều tăng lên bằng cách tăng 10 - 20 ng/kg/phút sau mỗi 15 phút dựa trên đáp ứng lâm sàng; một khi bệnh nhân ổn định và quyết định ngừng liệu pháp, điều chỉnh liều giảm xuống bằng cách giảm 10 ng/kg/phút sau mỗi 2 giờ dựa trên đáp ứng lâm sàng; liều tối đa 50 ng/kg/phút.
Bệnh nhân ARDS với:
- Tình trạng bệnh nền yêu cầu glucocorticoid toàn thân:
- ARDS là hậu quả của tiến triển của tình trạng đáp ứng với steroid (ví dụ: viêm phổi do tăng bạch cầu ái toan, viêm phổi tổ chức hóa).
- ARDS liên quan với sốc nhiễm trùng kháng trị.
- ARDS liên quan đến COVID-19.
- ARDS liên quan đến viêm phổi mắc phải cộng đồng (cần thở máy không xâm lấn hoặc xâm lấn hoặc P/F < 300 mmHg với FiO2 ≥ 50% khi sử dụng HFNC hoặc mask túi không hít lại) không phải nguyên nhân do cúm/lao/nấm, không nên sử dụng cho bệnh nhân nhiễm virus viêm gan B, herpes đang hoạt động, cân nhắc cá thể hóa ở bệnh nhân suy giảm miễn dịch.
- Bệnh nhân ARDS mức độ trung bình đến nặng (P/F < 200 mmHg) ở giai đoạn tương đối sớm (trong vòng 14 ngày từ khi khởi phát triệu chứng) thất bại với các liệu pháp tiêu chuẩn(bao gồm cả thông khí Vt thấp).
- Methylprednisolone 1 mg/kg/ngày (theo cân nặng lý tưởng) IV chia thành nhiều lần trong 14 ngày, sau đó giảm dần liều trong tổng thời gian điều trị 21 - 28 ngày.
- Dexamethasone 20 mg IV một lần duy nhất trong ngày trong 5 ngày đầu, sau đó 10 mg một lần duy nhất trong ngày trong 5 ngày tiếp theo.
- ARDS nhẹ P/F ≥ 200 mmHg không sử dụng một cách thường quy.
- ARDS giai đoạn muộn > 14 ngày kể từ khi khởi phát, có thể có hại, tăng tỷ lệ tử vong. Ở những bệnh nhân ARDS kháng trị/ dai dẳng > 14 ngày có thể thực hiện các chẩn đoán bổ sung (ví dụ: nội soi phế quản, sinh thiết phổi) để tìm nguyên nhân có thể khác, liệu pháp Glucocorticoid trong giai đoạn này có thể phù hợp ở một số bệnh nhân như viêm phổi tổ chức hóa.
- Bệnh nhân nhiễm cúm: có thể dẫn đến kết cục tồi tệ.
Tránh an thần quá mức và nên sử dụng các thang điểm để đạt được mức an thần nhẹ. Xem thêm:
- An thần, giảm đau, giãn cơ trong thở máy, ICU.
- NPRS (Numerical Pain Rating Scale) thang xếp hạng mức độ đau theo số cho bệnh nhân tự chọn khi không thể nói(rối loạn phát âm, đặt nội khí quản,..)
- Behavioral Pain Scale (BPS) đánh giá mức độ đau dựa trên hành vi.
- CPOT (Critical Care Pain Observation Tool) công cụ đánh giá đau dựa trên quan sát ở bệnh nhân hồi sức tích cực
- RASS (Richmond Agitation Sedation Scale) thang điểm an thần kính động Richmond dành cho bệnh nhân đặt nội khí quản thở máy
- SAS (Sedation Agitation Scale) Riker thang điểm an thần kích động Riker
- RAMSAY Sedation Scale thang điểm an thần RAMSAY
Bệnh nhân ARDS theo dõi các dấu hiệu sinh tồn và hệ thống kết nối qua màn hình trung tâm. Việc theo dõi huyết động có thể cần phải đặt catheter động mạch và tĩnh mạch trung tâm, đặc biệt với việc sử dụng PICCO giúp quản lý dịch trong phổi hiệu quả hơn. Tuy nhiên việc sử dụng catheter động mạch phổi thường quy với dữ liệu hiện tại đã không còn được khuyến cáo. Siêu âm tại giường để theo dõi huyết động được sử dụng ngày càng nhiều để quản lý dịch(đường B trên siêu âm phổi, độ xẹp IVC, CO siêu âm tim qua thành ngực) ở bệnh nhân sốc. Xem thêm:
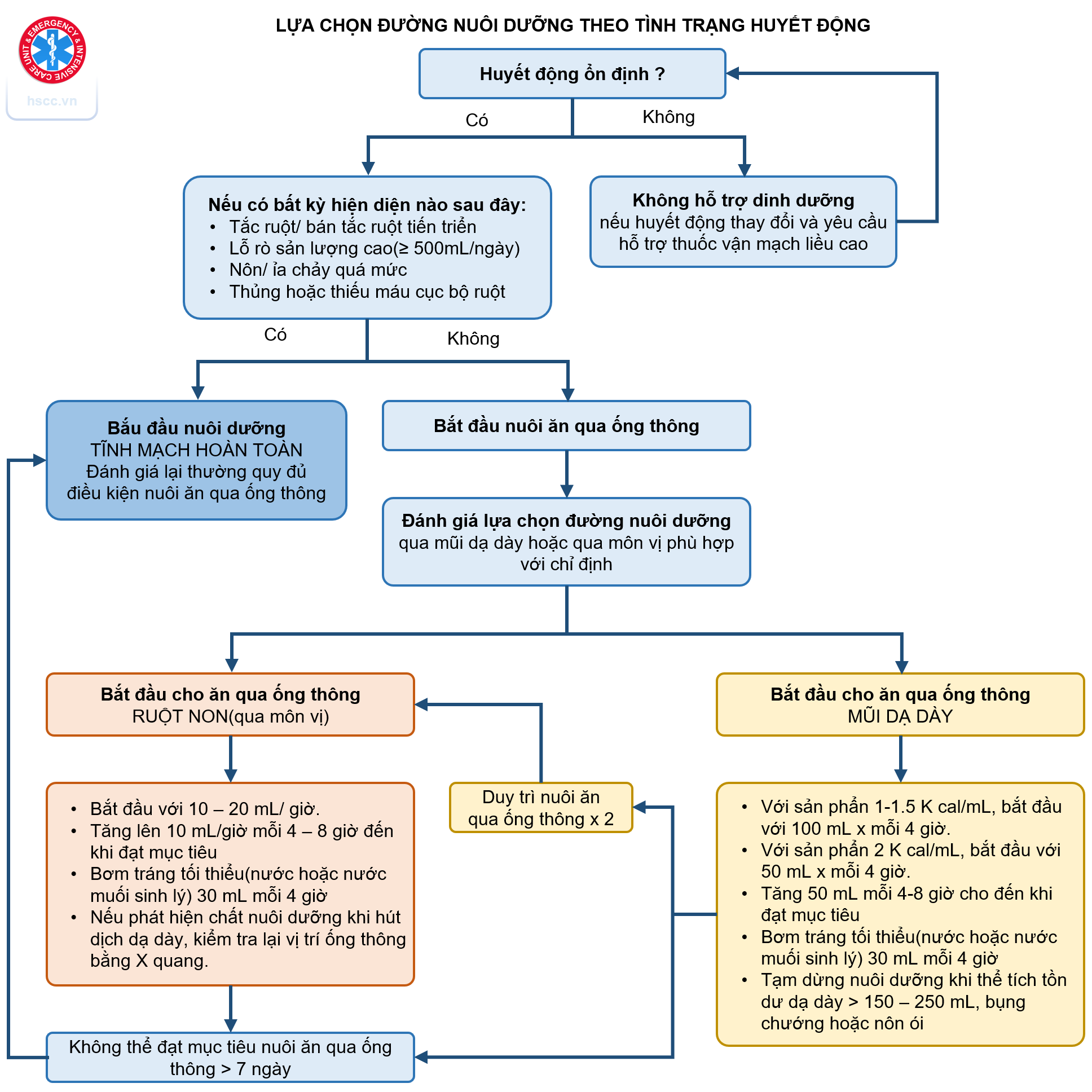
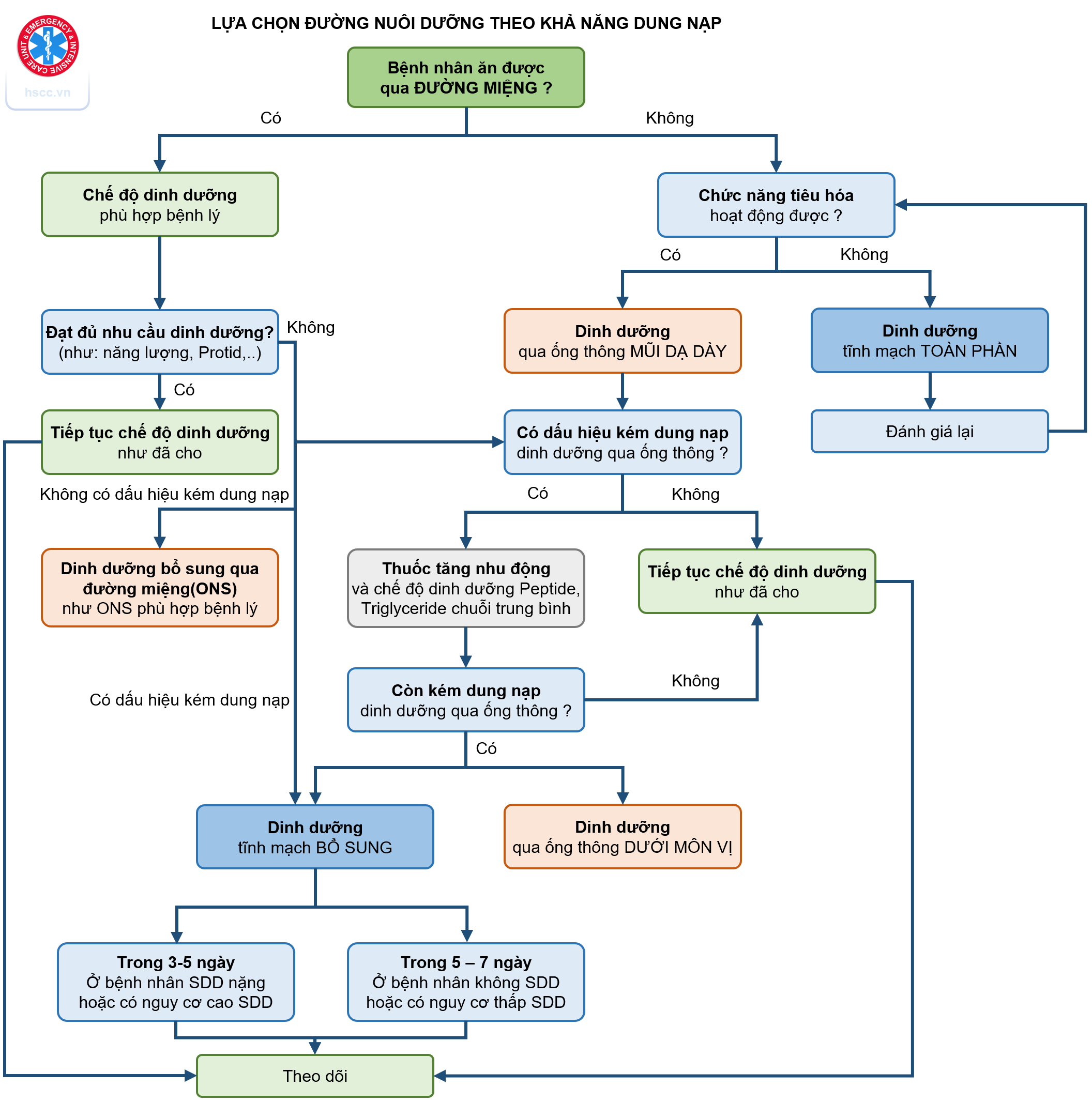
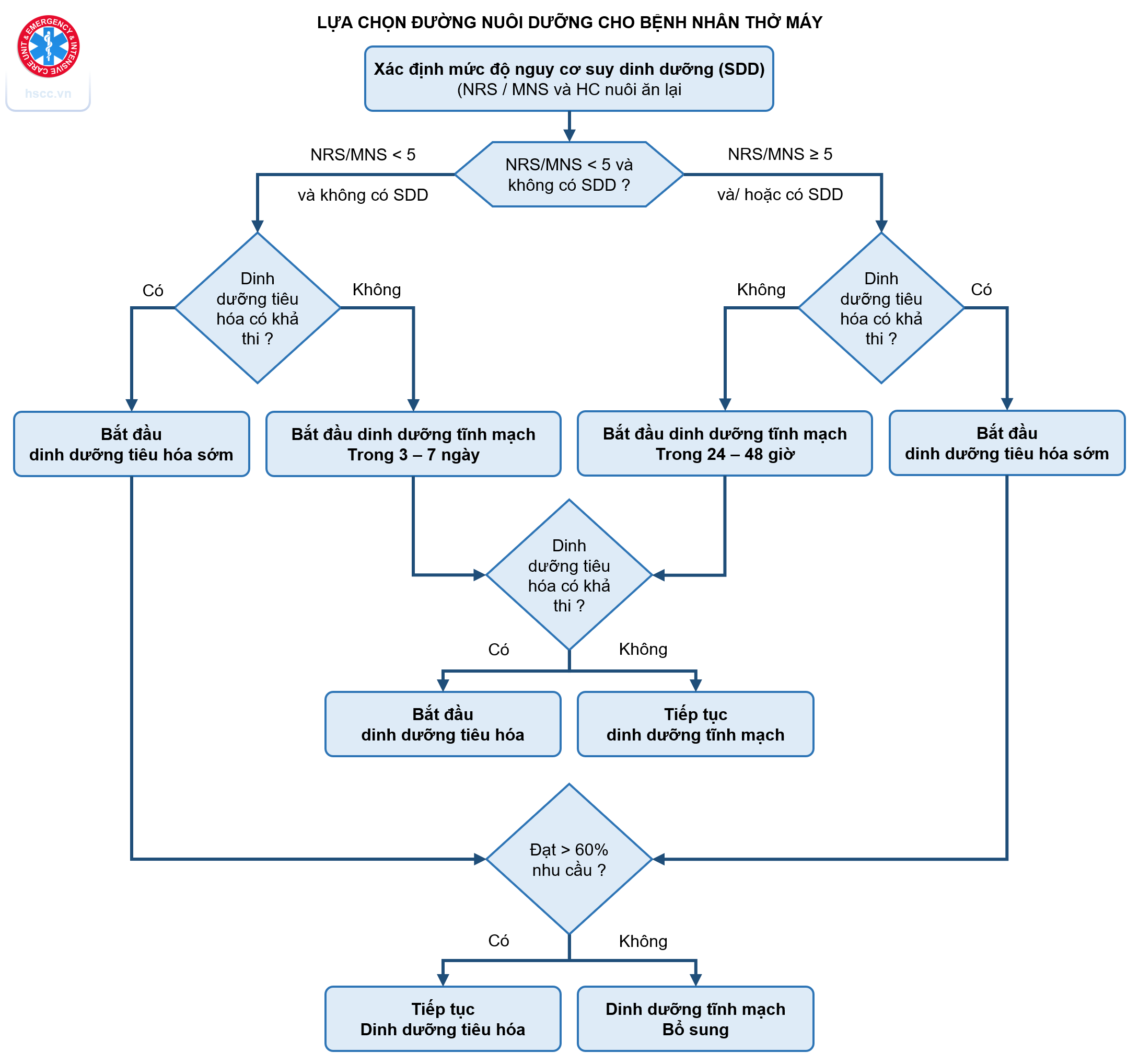
Bệnh nhân ARDS dị hóa mạnh và hỗ trợ dinh dưỡng có thể giúp bù đắp sự mất mất do quá trình dị hóa này và điều chỉnh đáp ứng trao đổi chất với stress, giảm thiểu tổn thương tế bào do oxy hoá, và thúc đẩy các đáp ứng miễn dịch có lợi. Xem thêm: Dinh dưỡng trong HSCC.
Trong hầu hết các khuyến cáo nên duy trì mức đường huyết 7.7 - 10.0 mmol/L(140 - 180 mg/dL), một mức đường huyết có thể chấp nhận được 6.0 - 10 mmol/L và tránh hạ đường huyết. Xem thêm: Kiểm soát đường huyết trong HSCC
Phòng ngừa viêm phổi bệnh viện và gói VAP bundle để phòng ngừa viêm phổi do thở máy.
Ở những bệnh nhân ARDS thường có nhiều yếu tố nguy cơ gây huyết khối tĩnh mạch, bao gồm bất động kéo dài, chấn thương, và có khuynh hướng bệnh nặng như: nhiễm trùng huyết, béo phì, và bệnh ác tính. Xem thêm: Dự phòng thuyên tắc huyết khối tĩnh mạch ở bệnh nhân điều trị tích cực (ICU).
Bệnh nhân ARDS cần thở máy kéo dài có nguy cơ cao bị xuất huyết tiêu hóa và cần điều trị dự phòng loét dạ dày do stress. Xem thêm: Tiêu chuẩn dự phòng xuất huyết tiêu hóa ở bệnh nhân hồi sức theo BMJ.
Trong khi đường truyền tĩnh mạch ngoại vi là hình thức tiếp cận nhanh để xử trí ban đầu, nhưng bệnh nhân ARDS nặng đường truyền tĩnh mạch trung tâm (CVC) có nhiều lợi thế bổ sung như: sử dụng thuốc vận mạch, lấy máu xét nghiệm, đo CVP, truyền dung dịch ưu trương, dinh dưỡng tĩnh mạch... Việc chăm sóc đường truyền trung tâm để phòng ngừa nhiễm trùng huyết liên quan đến đường truyền trung tâm có thể áp dụng gói Central Line Bundle. Ngoài đường truyền tĩnh mạch, đường truyền động mạch cũng có thể được sử dụng trong trường hợp theo dõi huyết động, lấy máu làm khí máu thường xuyên.
Bằng chứng hiện tại cho thấy rằng việc sử dụng thuốc tiêu nhày (long đàm) thường quy không có vai trò gì trong ARDS.
- Việc xử trí sốt tương tự như những bệnh nhân ICU khác.
Xem thêm: Chỉ định truyền máu và chế phẩm máu.
Do tính chất tiến triển nhanh chóng và tỷ lệ tử vong cao liên quan đến ARDS, kháng sinh thường được bắt đầu theo kinh nghiệm tùy theo nguyên nhân. Ở những bệnh nhân ARDS đã tiếp xúc với kháng sinh trước đó và sự thay đổi của hệ vi sinh vật ở phổi thường rất phức tạp do các vi sinh vật đa kháng thuốc, chẳng hạn như: Staphylococus aureus (tụ cầu vàng), Pseudomonas aeruginosa (trực khuẩn mủ xanh), và Acinetobacter, liên quan đến kết cục xấu. Xem thêm:
TÀI LIỆU THAM KHẢO
0 , 0 bình luận
7092 lượt xem